[Gradient phases of the transimpedance matrix as an indicator of the insertion depth of cochlear implants]
Florian Herrmann Schmidt 1Lichun Zhang 1
Karsten Ehrt 1
Wilma Großmann 1
Robert Mlynski 1
1 Klinik und Poliklinik für Hals-Nasen-Ohrenheilkunde, Kopf- und Halschirurgie „Otto Körner“, Universitätsmedizin Rostock, Deutschland
Abstract
Introduction: The insertion depth of cochlear implants (CIs) plays a crucial role in auditory perception, as the final position of the electrode array determines which frequency-specific neural structures are stimulated. The Slim Straight Electrode from Cochlear Ltd. enables surgeons to vary the insertion depth during implantation to best suit the individual anatomical and clinical needs of each patient. However, there are currently no clear intraoperative reference points to indicate when the desired insertion depth has been achieved. Transimpedance measurement is a fast, radiation-free electrophysiological technique that may offer a viable method for estimating insertion depth.
Methods: Intraoperative transimpedance measurements were performed in 39 patients. Gradient fields were derived from the resulting transimpedance matrices (TIM), and the phases of these gradients were correlated with the insertion depths as determined postoperatively by radiological imaging.
Results: A strong correlation (R=0.80) was observed between insertion depth and gradient phase. Notably, electrode pairs located in the apical-medial region had the greatest influence on determining insertion depth.
Conclusion: Intraoperative transimpedance measurement is an effective method for assessing the insertion depth of cochlear implant electrodes. It offers valuable intraoperative guidance, particularly for electrode arrays with variable insertion depths, such as Cochlear’s Slim Straight electrode.
Keywords
cochlear implant, insertion depth, transimpedance matrix
Einleitung
Die Insertionstiefe von Cochlea-Implantaten (CI) ist ein entscheidender Faktor für die Qualität der auditorischen Wahrnehmung. Sie bestimmt maßgeblich, welche frequenzspezifischen neuronalen Strukturen in der Cochlea durch elektrische Stimuli angeregt werden, und beeinflusst somit direkt das Sprachverstehen und das subjektive Hörerlebnis [1].
Besonders das Design der Slim-Straight-Elektrode (CI622, Cochlear Ltd.) ermöglicht eine variabel steuerbare Einführtiefe, wodurch der Chirurg intraoperativ Spielraum für eine anatomiegerechte Platzierung erhält. Farbige Markierungen am Elektrodenträger zeigen an, welcher Abschnitt in Höhe des runden Fensters positioniert werden sollte. Bisher fehlen jedoch standardisierte, objektive Verfahren, mit denen sich intraoperativ exakt diejenige Position bestimmen lässt, die der zuvor definierten Insertionstiefe entspricht.
Informationen über die endgültige Lage des Elektrodenträgers werden derzeit überwiegend postoperativ mittels radiologischer Bildgebung gewonnen. Diese Verfahren sind jedoch mit einer Strahlenbelastung verbunden und liefern im Regelfall keine unmittelbare Rückmeldung während des operativen Eingriffs.
Die Messung der Transimpedanzmatrix (TIM) stellt in diesem Zusammenhang eine vielversprechende Alternative dar: Sie ist strahlenfrei, schnell durchführbar und prinzipiell intraoperativ einsetzbar [2].
Sie basiert auf der Analyse elektrischer Feldverteilungen zwischen benachbarten Elektrodenpaaren [3] und ermöglicht eine indirekte Bestimmung der Elektrodenposition innerhalb der Cochlea [4], [5]. Besonders effektiv ist dies bei der Auswertung charakteristischer Muster anhand von Gradientenphasen [6]. Anhand charakteristischer Muster in der TIM lassen sich Fehllagen des Elektrodenträgers in der Cochlea mit hoher Sensitivität nachweisen [7], [8].
Ziel der vorliegenden Studie ist es, die Eignung der TIM zur intraoperativen Abschätzung der Insertionstiefe systematisch zu untersuchen. Dabei steht insbesondere die Auswertung der Gradientenphasen im Fokus – ein Ansatz, bei dem Veränderungen der elektrischen Feldverteilung entlang benachbarter Elektroden genutzt werden, um Rückschlüsse auf die Position und Tiefe des Elektrodenträgers innerhalb der Cochlea zu ermöglichen [6], [7].
Methode
In dieser retrospektiven Studie wurden zwischen 2022 und 2024 Daten von Patienten erhoben, die mit einer Slim-Straight-Elektrode (CI622, Cochlear Ltd.) versorgt wurden und bei denen intraoperative Transimpedanzmessungen durchgeführt wurden. Die Elektroden wurden über eine Rundfenster-Insertion im Rahmen einer transmastoidalen posterioren Tympanotomie implantiert. Die Einführung erfolgte gemäß Herstellerempfehlung bis etwa zur Mitte zwischen den beiden weißen Markierungen des Elektrodenträgers.
Die TIM-Daten wurden unmittelbar nach vollständiger Insertion mit der Software CustomSound EP (Version 6.0, Cochlear Ltd.) aufgezeichnet. Es wurde eine vollständige 22x22 Transimpedanzmatrix erhoben, indem nacheinander jede der 22 Elektroden als Stimulator diente und die jeweils übrigen als Empfänger. Die Messungen erfolgten mit der maximal möglichen Stromstärke (196–223 CL, die von Custom Sound EP automatisch aus der Compliance-Grenze berechnet wird und patientenabhängig variiert. Die Impulsparameter umfassten eine Pulsbreite von 25 µs und einen Inter-Phase-Gap von 9 µs.
Aus der TIM wurde mithilfe der Software MATLAB version R2014a (MathWorks, Natick, MA) ein zweidimensionales Gradientenfeld berechnet. Da die TIM mit konstanten Stromstärken gemessen wurde, lässt sich aus dem berechneten Gradientenfeld das elektrische Potentialfeld φ konstruieren. Dieses steht in direktem Zusammenhang mit den Stromquellen, da deren Position und Stärke die räumliche Verteilung des Potentials bestimmen. Der Gradient des Potentials ergibt das elektrische Feld 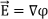 , das den Verlauf der Stromlinien zwischen den Injektions- und Ableitpunkten beschreibt. Die Richtung des Gradientenfeldes gibt dabei den Verlauf der Feldlinien an, die von den Strominjektionspunkten ausgehen und zu den Ableitpunkten hin verlaufen. Eine Veränderung des Elektrodenabstands infolge einer Krümmung des Elektrodenträgers führt zu Verzerrungen des elektrischen Feldes, die sich in den Richtungen (Phasen) der Gradientenvektoren widerspiegeln. Die Gradienten wurden in Polarkoordinaten transformiert und normiert, um die Gradientenphasen zu extrahieren, woraus eine Gradientenphasenmatrix resultierte (vgl. Abbildung 1 [Abb. 1]).
, das den Verlauf der Stromlinien zwischen den Injektions- und Ableitpunkten beschreibt. Die Richtung des Gradientenfeldes gibt dabei den Verlauf der Feldlinien an, die von den Strominjektionspunkten ausgehen und zu den Ableitpunkten hin verlaufen. Eine Veränderung des Elektrodenabstands infolge einer Krümmung des Elektrodenträgers führt zu Verzerrungen des elektrischen Feldes, die sich in den Richtungen (Phasen) der Gradientenvektoren widerspiegeln. Die Gradienten wurden in Polarkoordinaten transformiert und normiert, um die Gradientenphasen zu extrahieren, woraus eine Gradientenphasenmatrix resultierte (vgl. Abbildung 1 [Abb. 1]).
Abbildung 1: Darstellung der Gradienten der TIM als Heatmap. Die Winkel der Gradientenphasen sind so normiert, dass Pfeile orthogonal zur Hauptdiagonalen einem Winkel von 0° entsprechen. Die Beträge der Gradienten wurden zur besseren Visualisierung auf den Wert 1 normiert und nicht in die Berechnungen einbezogen.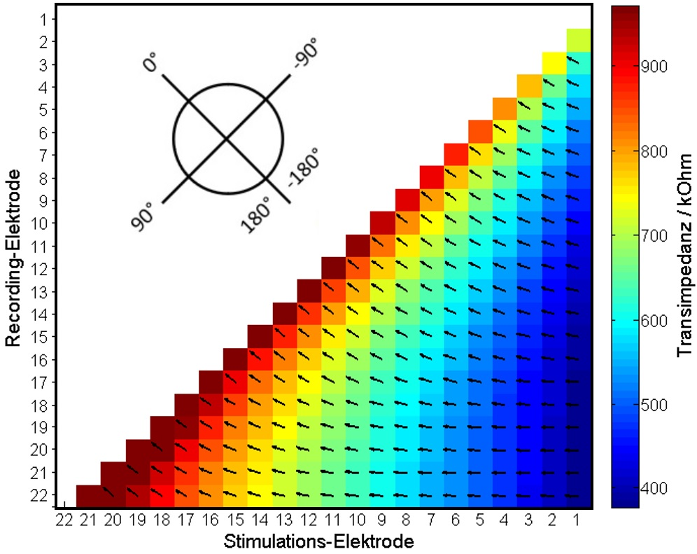
Zur Validierung der TIM-Daten wurden die maximalen angularen Insertionstiefen (maxAID) aus postoperativen Röntgenaufnahmen in Stenvers-Projektion bestimmt. Die Elektrodenpositionen wurden manuell mithilfe der Software 3D Slicer (https://www.slicer.org) identifiziert. Aufgrund möglicher projektionsbedingter Abweichungen ist die Stenvers-Projektion weniger genau als eine Computertomografie (CT), auf die jedoch postoperativ zur Verringerung der Strahlenbelastung meist verzichtet wird. Anschließend wurden die radiologisch ermittelten maxAID-Werte mit den Einträgen der Gradientenphasenmatrix korreliert (Pearson-Korrelation). Zur Kontrolle multipler Testungen wurde eine Bonferroni-Korrektur auf die berechneten p-Werte angewendet. Die Signifikanzniveaus wurden wie folgt klassifiziert: signifikant (p<0,05), stark signifikant (p<0,01) und hochsignifikant (p<0,0001).
Ergebnisse
In die Studie wurden 39 Patienten eingeschlossen. Die mittlere maxAID betrug 334,2°±44,3°. Die TIM-Messung erfolgte bei einem durchschnittlichen Stimulationsniveau von 213,8 CL ±12,0CL, woraus sich mittlere Transimpedanzwerte von 655,6 kΩ ±253,2 kΩ ergaben.
Es zeigte sich eine signifikante Korrelation zwischen den Gradientenphasen der TIM und der Insertionstiefe (Abbildung 2 [Abb. 2]). Insgesamt wiesen 154 Elektrodenpaare signifikante, 136 stark signifikante und 61 hochsignifikante Zusammenhänge mit der maxAID auf. Die signifikante Korrelation betraf Elektroden, die apikal im Bereich von E17 bis E21 lagen, während die jeweils zugehörigen Partner-Elektroden variabler positioniert waren, typischerweise zwischen E2 und E17.
Abbildung 2: Korrelationsmatrix zwischen der maximalen angularen Insertionstiefe (maxAID) des Elektrodenträgers und den Gradientenphasen der intraoperativ gemessenen TIM. Signifikante Bereiche sind farblich hervorgehoben, wobei die Rahmenfarben die jeweiligen Signifikanzniveaus kennzeichnen (schwarz: p<0,05; magenta: p<0,01; weiß: p<0,0001).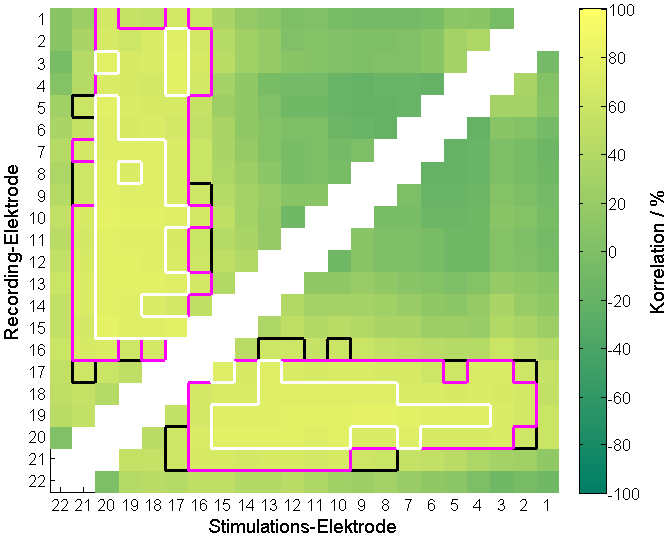
Die höchste Korrelation wurde für das apikal-mediale Elektrodenpaar E20–E10 mit einem Korrelationskoeffizienten von R=0,798 (p<0,0001) festgestellt (Abbildung 3 [Abb. 3]).
Abbildung 3: Vergleich der maximalen Insertionstiefe (maxAID) des Elektrodenträgers mit der Gradientenphase des Elektrodenpaars E20–E10, das in der Korrelationsmatrix die höchsten Korrelationswerte aufweist. Es zeigt sich eine positive Korrelation zwischen maxAID und der Gradientenphase (R=0,798, p<0,0001).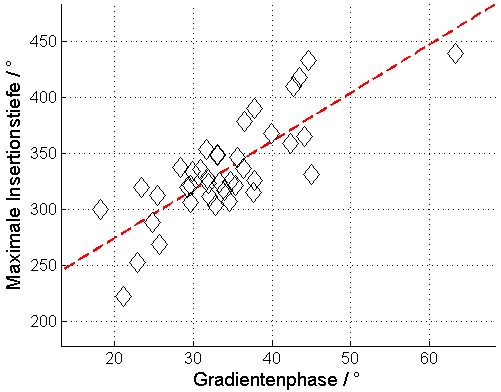
Zusammenfassung und Schlussfolgerung
Die vorliegende Studie bestätigt die intraoperativ gemessene TIM als effektive Methode zur Bestimmung der Insertionstiefe von geraden Elektroden, wie der CI622. Besonders im Kontext der Slim-Straight-Elektrode von Cochlear, die eine variabel steuerbare Einführtiefe erlaubt, stellt TIM ein wertvolles intraoperatives Instrument zur Orientierung und Entscheidungsfindung dar. Dies ist umso relevanter, da etablierte bildgebende Verfahren wie CT oder Röntgen zwar zur Lagebestimmung geeignet sind, jedoch in der Regel nicht in Echtzeit verfügbar sind und mit zusätzlicher Strahlenexposition einhergehen.
Die Analyse der TIM-Daten, insbesondere der Gradientenphasen der TIM, zeigte eine signifikante Korrelation mit der Insertionstiefe des Elektrodenträgers. Eine besonders hohe Korrelation zeigte sich beim Elektrodenpaar E20–E10 (R=0,798, p<0,0001). Insgesamt wurden 154 signifikant korrelierte Elektrodenpaare identifiziert.
Auffällig ist, dass die Korrelation mit der maxAID nicht auf einzelne Elektrodenpaare beschränkt war, sondern eine robuste Korrelation über mehrere Paarungen hinweg vorlag. Allerdings zeigte sich, dass eine verlässliche Schätzung der maxAID nur gelang, wenn eine apikal positionierte Elektrode vorhanden war (zumindest zwischen E17 und E21). Dieser Befund könnte damit zusammenhängen, dass die maxAID die Position der apikalsten Elektrode widerspiegelt. Da jedoch die AID basaler Elektroden direkt mit der maxAID korreliert, könnte dieser Befund auch auf potenzielle Einschränkungen bei der Anwendung der Gradientenphasen-Analyse der TIM hinweisen – insbesondere in der frühen Phase der Implantation. Es muss demnach zunächst eine ausreichend tiefe Insertion erfolgen, um die apikalen Regionen zu erreichen, in denen die maxAID gemäß den Ergebnissen dieser Studie zuverlässig korreliert. Erst dann sind aussagekräftige Schätzungen der maxAID möglich. Dies würde die Verwendbarkeit der TIM-Messungen als simultanes Monitoring der Insertionstiefe während der Implantation erheblich einschränken.
Eine weitere Einschränkung der Ergebnisse ist die hohe Streuung der geschätzten Insertionstiefe, die auf dem linearen Regressionsmodell basiert (Abbildung 3 [Abb. 3]) und teilweise etwa 50° beträgt – das entspricht ungefähr einer Achtel Windung. Im Verhältnis zur durchschnittlichen maxAID von 334° ist dies mit rund 15% relativ hoch. Für präzise Implantationen, bei denen bestimmte frequenzspezifische Strukturen zum Erhalt des Restgehörs geschont werden sollen, könnte dieses Verfahren daher noch zu ungenau sein.
Insgesamt bestätigen die Ergebnisse das Potenzial der TIM als intraoperative Methode zur optimierten Steuerung der Insertionstiefe – insbesondere bei Implantaten mit variabler Insertionstiefe wie der Slim-Straight-Elektrode. Gleichzeitig werden die Grenzen der Methode bei der Anwendung während des unmittelbaren Insertionsverlaufs deutlich.
Anmerkungen
Konferenzpräsentation
Dieser Kurzbeitrag wurde bei der 27. Jahrestagung der Deutschen Gesellschaft für Audiologie präsentiert und als Abstract veröffentlicht [9].
Interessenkonflikte
Die Autorinnen und Autoren erklären, dass keine Interessenkonflikte in Zusammenhang mit diesem Artikel bestehen.
Literatur
[1] Kurz A, Müller-Graff F, Hagen R, Rak K. One Click is not enough: anatomy-based fitting in experienced cochlear implant users. Otol Neurotol. 2022;43(10):1176-80. DOI: 10.1097/MAO.0000000000003731[2] Van Poucke FJ, Boermans PB, Frijns JH. Assessing the placement of a cochlear electrode array by multidimensional scaling. IEEE Trans Biomed Eng. 2012;59:307-10. DOI: 10.1109/TBME.2011.2173198y
[3] Kopsch AC, Rahne T, Plontke SK, Wagner L. Influence of the spread of electric field on neural excitation in cochlear implant users: Transimpedance and spread of excitation measurements. Hear Res. 2022 Oct;424:108591. DOI: 10.1016/j.heares.2022.108591
[4] Aebischer P, Meyer S, Caversaccio M, Wimmer W. Intraoperative impedance-based estimation of cochlear implant electrode array insertion depth. IEEE Trans Biomed Eng. 2021;68:545-55. DOI: 10.1109/TBME.2020.3006934
[5] Schraivogel S, Aebischer P, Wagner F, Weder S, Mantokoudis G, Caversaccio M, Wimmer W. Postoperative Impedance-Based Estimation of Cochlear Implant Electrode Insertion Depth. Ear Hear. 2023 Nov-Dec 01;44(6):1379-88. DOI: 10.1097/AUD.0000000000001379
[6] Zhang L, Schmidt FH, Oberhoffner T, Ehrt K, Cantré D, Großmann W, Schraven SP, Mlynski R. Transimpedance Matrix Can Be Used to Estimate Electrode Positions Intraoperatively and to Monitor Their Positional Changes Postoperatively in Cochlear Implant Patients. Otol Neurotol. 2024 Apr 1;45(4):e289-e296. DOI: 10.1097/MAO.0000000000004145
[7] Hoppe U, Brademann G, Stöver T, Ramos de Miguel A, Cowan R, Manrique M, Falcón-González JC, Hey M, Baumann U, Huarte A, Liebscher T, Bennett C, English R, Neben N, Ramos Macías A. Evaluation of a Transimpedance Matrix Algorithm to Detect Anomalous Cochlear Implant Electrode Position. Audiol Neurootol. 2022;27(5):347-55. DOI: 10.1159/000523784
[8] Franke-Trieger A, Lailach S, Strahl SB, Murrmann K, Schebsdat E, Neudert M, Zahnert T. Voltage Matrix Algorithm for Intraoperative Detection of Cochlear Implant Electrode Misplacement. Audiol Neurootol. 2025;30(3):252-62. DOI: 10.1159/000543264
[9] Schmidt FH, Zhang L, Ehrt K, Großmann W, Mlynski R. Gradientenphasen der Transimpedanzmatrix als Indikator für die Insertionstiefe von Cochlea-Implantaten. In: Deutsche Gesellschaft für Audiologie e. V.; ADANO, editors. 27. Jahrestagung der Deutschen Gesellschaft für Audiologie und Arbeitstagung der Arbeitsgemeinschaft Deutschsprachiger Audiologen, Neurootologen und Otologen. Göttingen, 19.-21.03.2025. Düsseldorf: German Medical Science GMS Publishing House; 2025. Doc069. DOI: 10.3205/25dga069




